
على مدى العقود الماضية من مسيرتي المهنية، أمضيت ساعات لا حصر لها في العمل على حماية الأميركيين من خلال البحث في سلامة الأدوية. لقد أخذني تعليمي وحياتي المهنية إلى ما يقرب من ست جامعات، وشركات الأدوية الكبرى، وإدارة الغذاء والدواء تحت ثلاث إدارات رئاسية. تأخذ سلامة الأدوية بعين الاعتبار الأسباب التي تجعل فردًا ما يتناول منتجًا صيدلانيًا ولا يكون لديه أي آثار جانبية، في حين يمكن لشخص آخر أن يتناول نفس المنتج ولكن يكون له ردود فعل سلبية تصل إلى العجز الدائم أو الوفاة. بشكل افتراضي، تأخذ دراسة سلامة الأدوية في الاعتبار أيضًا الجوانب غير السريرية للتصنيع وجودة الدواء أيضًا.
ونظرًا لأن جودة الدواء عامل أساسي في تقييم سلامة الدواء، فقد أدت رحلتي لحماية الأمريكيين إلى وضع تصور وتأسيس أول شركة في العالم "صيدلية تحليليةمهمتها التحقق علميًا من المنتجات الصيدلانية الواردة من أماكن مثل الهند والصين قبل توزيعها على المرضى. ولسوء الحظ، أدى السعي وراء السخاء على الأخلاق وحماية المرضى إلى التزام الإدارة المالية لتلك الشركة واسع انتهاكات ادارة الاغذية والعقاقير واتهامهم من قبل القضاة بصنع ادعاءات علمية كاذبة (كل ذلك حدث بالصدفة بعد خروجي).
بدون تأكيد خارجي لجودة الدواء، يعتمد الأمريكيون بشكل كامل على إدارة الغذاء والدواء والمصنعين لتقييم وتأكيد نقاء المنتج. لقد ثبت أن سلامة الأدوية تمثل مشكلة جديرة بالملاحظة عندما يتعلق الأمر بحقن Covid mRNA. لسوء الحظ، إذا أراد أي شخص إجراء تحليله الخاص على حقن mRNA، فإنه ليس لديك قائمة مكونات مفصلة بشكل مناسب لمقارنتها، أو حتى الوصول إلى المنهجية التنظيمية المعمول بها حول كيفية اختبار النقاء بشكل صحيح.
ذلك لأن الشركات المصنعة و تأخذ إدارة الغذاء والدواء في الاعتبار جميع مكونات حقن mRNA هذه، بما في ذلك تسلسل mRNA بالإضافة إلى خصائص الجسيمات الدهنية النانوية (LNP) بما في ذلك عمر النصف، وهياكل LNP، وتعديلات السطح، وعدد/أنواع LNPs لكل جرعة ونقاط التعلق على حبلا mRNA، غير محدد أو "سر تجاري".
علاوة على ذلك، تعتبر إدارة الغذاء والدواء الأمريكية (FDA) أيضًا المنهجيات حول كيفية اختبار حقن mRNA من أجل النقاء، وهو سر تجاري أيضًا.
دعم الحزبين ومئات المليارات من دولارات دافعي الضرائب، ولكن لا توجد شفافية؟
توجد سرية Covid mRNA على الرغم من أن كلاً من إدارات ترامب وبايدن اقترحت الشفافية الكاملة مع حقن mRNA إلى درجة رفع حقوق الملكية الفكرية لـ Covid mRNA. على الرغم من ذلك، فإن إدارة الغذاء والدواء الأمريكية والمصنعين يسمحون/يحافظون على قبضتهم الصارمة على براءات الاختراع، بما في ذلك البيانات الأساسية حول هذه اللقطات، باعتبارها سرًا تجاريًا. إنهم يفعلون ذلك على الرغم من حصول جميع الشركات المصنعة للقاح كوفيد مئات الملايين من دولارات دافعي الضرائب بالنسبة الى فوربس / ستاتيستا المنشورات.
إن دراسة علم الأوبئة المتعلقة بسلامة الأدوية أمر صعب بما فيه الكفاية. وبدون التحقق من نقاء/اتساق المنتج، يكون تقييم السلامة الكامل مستحيلاً.
إن الشفافية الكاملة لجميع المكونات وتدابير مراقبة الجودة مهمة ليس فقط لأنها تم تمويلها بشكل كبير من قبل دافعي الضرائب بمئات الملايين من الدولارات، ولكن بسبب عدد كبير من الأسئلة التي نشأت حول سلامة وفعالية حقن فيروس كورونا المرسال.
بالإضافة إلى كونها معقدة بشكل استثنائي، تم التعجيل بالموافقة عليها من قبل المنظمين بعد ذلك اقل من عام واحد. عادةً ما تستغرق معظم الأدوية واللقاحات وقتًا طويلاً عشر سنوات لاختبار كامل للسلامة/الفعالية ومراجعتها والموافقة عليها. بالإضافة إلى كون المكونات جديدة تمامًا، ومعقدة للغاية، والأولى من نوعها التي يتم تطبيقها على نطاق واسع، بما في ذلك التطوير تم التعجيل بتقييمات السلامة / السمية السريرية طويلة المدى ومراجعات الأوبئة ومن المحتمل ألا يتم توضيحها بشكل كامل قبل الإصدار.
إن التحقق من المكونات والشفافية و"الصدق" لدى إدارة الغذاء والدواء لها سوابق يعود تاريخها إلى القرن التاسع عشر:
التحقق التحليلي وشفافية المكونات أو "الحقيقة في وضع العلامات" على محتويات الزجاجة مطلوب لتتناسب مع المكونات المذكورة يسبق إنشاء إدارة الغذاء والدواء الأمريكية (FDA)، ويعود إلى عام 1862. لقد ولدت إدارة الغذاء والدواء اليوم في واقع الأمر نتيجة لما بدأ كموظف واحد في "قسم الكيمياء" يعمل في وزارة الزراعة الأمريكية.
غش، (المكونات المعدلة أو السامة) علامة تجارية خاطئة (يحتوي على تسمية زائفة أو مضللة بأي شكل آخر، أو يحتوي على ادعاءات طبية غير صحيحة)، أو تسمية خاطئة (يحتوي على مكون (مكونات) غير مدرجة في ملصق المنتج) كان لها جميعًا تاريخ طويل وقبيح في أمريكا. كان يُعتقد أن الفظاعة قد بلغت ذروتها في أوائل القرن التاسع عشر وحتى منتصفه - أو على الأقل عندما أصبح من الممكن التعرف عليها - حيث أنه بحلول عام 19 فقط تم تطوير العمليات الفنية لتحليل واكتشاف الاحتيال في المكونات. قبل ذلك، كان ما يسمى بـ "رجال الطب المتنقلين" الذين يطلقون على أنفسهم اسم "أطباء" (بأوراق اعتماد مشكوك فيها أو غير موجودة دائمًا) يبيعون زجاجات تحتوي على منتجات "شفاء للجميع"، والتي لا تتضمن ملصقات مكوناتها سوى محتويات غامضة أو غير ضارة مثل "الفيتامينات""مستخلصات عشبية"أو"snake oil "- أو في كثير من الأحيان لا تحتوي على قائمة مكونات على الإطلاق.
في ذلك الوقت، كان العديد من سكان نيو إنجلاند المتدينين والمتشددين يفعلون ذلك لأسباب دينية أبدا لمس الكحول، سيشتري هذه المحاليل من هؤلاء الباعة المتجولين ويتم خداعه دون قصد في استهلاك المحاليل التي لا تحتوي على الكحول فحسب، بل تحتوي أيضًا على المخدرات مثل الأفيون و/أو الكوكايين. وتحت ذريعة تحسين مجموعة واسعة من الأمراض بشكل غير معقول، طور المرضى بدلاً من ذلك إدمانًا عقابيًا و/أو تأثرت صحتهم سلبًا بسبب "تجار المخدرات" الأوائل.
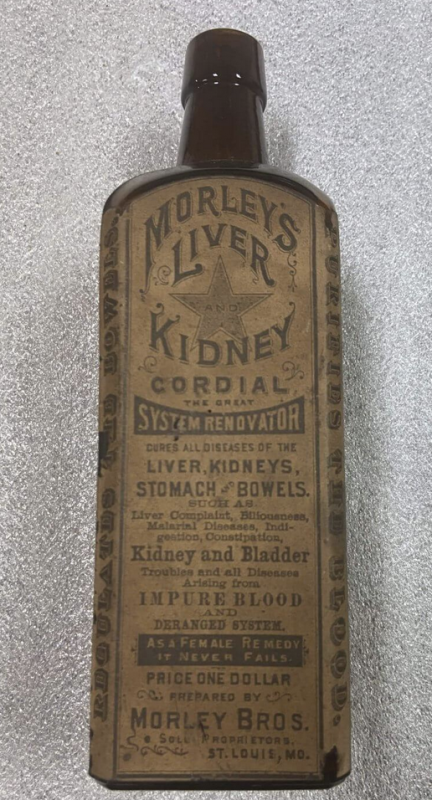
ومع تزايد المشكلة، بدأت الحكومة الفيدرالية في الانتباه. في نهاية المطاف، قانون الغذاء والدواء النقي صدر في عام 1906 وأدى إلى إنشاء إدارة الغذاء والدواء (FDA).
[كان لدى إدارة الغذاء والدواء أ تدريب واجب التأكد من أن الأدوية تحمل بيانات وصفية صادقة وتفي بمعايير معينة للنقاء والقوة.
تذكر أن ما يقرب من 120 عاما متطلبات وضع العلامات صادقة وجزء "النقاء" من قانون الغذاء والدواء النقي لعام 1906 أثناء قراءتك حول اختبار التحقق من mRNA وشفافية المكونات.]
ما هي اختبارات التحقق من المكونات "الصادقة" و"النقية" التي يتم إجراؤها للمنتجات الخاضعة لرقابة إدارة الأغذية والعقاقير (FDA)؟
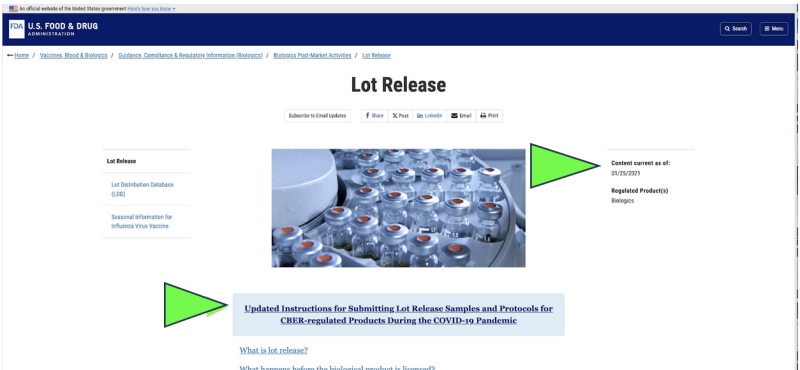
وبالعودة إلى عام 2021، اختارت إدارة الغذاء والدواء البدء في مراقبة جودة الأدوية الأمريكية عبر شبكة جمع عن بعد of إرسال العينات بالبريد للأدوية كبديل لعمليات التفتيش المباشر على المرافق بسبب جائحة كوفيد. هل كان ذلك قانونيًا؟ هل يمكن اعتبار ذلك مناسبًا علميًا؟ اليوم، على الرغم من انتهاء الوباء، يتم حاليًا إجراء الاختبار الرسمي الوحيد لإصدار الأدوية أي وقت أدوية كوفيد مرنا يبدو إلى لا يزال يتم إجراؤها بواسطة إدارة الغذاء والدواء الأمريكية (FDA) عبر منتج توفره الشركة المصنعة، "تم إرساله بالبريد" العينة وفقا ل لقطة شاشة لموقع إدارة الغذاء والدواء الحالي. من الواضح أن طريقة أخذ العينات "بالبريد" تختلف كثيرًا وربما تكون أقل موثوقية من جمع العينات مباشرة عبر طريقة جمع مباشرة وشخصية. وعلى الرغم من ذلك، تدعي إدارة الغذاء والدواء الأمريكية أنها "أعلى المعايير في جميع أنحاء العالم لأخذ العينات والاختبار".
علاوة على ذلك، تقترح إدارة الغذاء والدواء الأمريكية (FDA) مواصلة تطوير سياسة الاختبار عن بعد "بالبريد" من خلال أ وثيقة التوجيه المقترحة حديثا.
على الرغم من أنه موجود فقط كمسودة وثيقة لإدارة الغذاء والدواء، إلا أن المواقع الرسمية لإدارة الغذاء والدواء تظهر ذلك يبدو أن إرسال العينات بالبريد قد تم تنفيذه بالفعل منذ يناير 2021 على الأقل. يبدو أن إدارة الغذاء والدواء تؤكد نتائج تلك الاختبارات التي تم إرسالها بالبريد باعتبارها عملية تحقق مستقلة.
وعلاوة على ذلك، فإن أسفل الصفحة الأولى من مسودة إدارة الغذاء والدواء تقترح الوثيقة توسيع "الاختبار عن بعد". يسرد حاليا كل إدارة الغذاء والدواء (FDA) قسم تنظيم المنتجات في إدارة الغذاء والدواء (FDA)، مما يعني أنه مقترح سياسة على مستوى الوكالة.
القائمة الكاملة تتضمن ما يلي:
- مكتب الشؤون التنظيمية
- مكتب السياسات الغذائية والاستجابة
- مكتب المنتجات المختلطة
- مركز التقويم والبحوث البيولوجية
- مركز تقييم وبحوث المخدرات
- مركز الأجهزة والصحة الإشعاعية
- مركز سلامة الغذاء والتغذية التطبيقية
- مركز منتجات التبغ
- مركز الطب البيطري
هل تعتبر عينات مراقبة الجودة "المرسلة بالبريد" من قبل إدارة الغذاء والدواء مناسبة؟ ماذا لو كانت عمليات التفتيش على المطاعم التابعة لوزارة الصحة في الولايات تعكس سياسة إدارة الغذاء والدواء؟
تعد منهجية أخذ العينات "بالبريد" سخيفة بالمثل، على سبيل المثال، بالنسبة لإدارة الصحة في الولاية التي تراقب المطاعم من خلال مطالبتها بإرسال عناصر مختلفة من قائمتها بالبريد بشكل دوري إلى منشأة اختبار حتى تتمكن إدارات الصحة من اختبار المواد الغذائية المحتملة التلوث المولد، و/أو مطالبة المطاعم بالتعهد باختبار عناصر القائمة بنفسها. ماذا لو كان هذا المطعم في الصين؟ ماذا لو كان هذا المطعم في الهند؟ أو أي دولة أخرى معروفة بوجودها تاريخ سيء من الاحتيال ومراقبة الجودة مشاكل؟
قد تكون هذه المنهجية غير مقبولة لكل من المطاعم وشركات الأدوية، لأسباب تشمل ما هو واضح: يمكن للمصنعين إرسال العينات التي يفضلونها - وليس بالضرورة عينات تمثيلية. من الواضح أن الأمر ليس مثل حصول مفتشي إدارة الغذاء والدواء على عينات أثناء عمليات التفتيش غير المعلنة للمنشأة بأكملها.
تحت تشبيه المطعم، بالطبع جميع المطاعم ستفعل ذلك تقديم عينات من الدرجة "أ". والتي لن تكون بالضرورة ممثلة لما يتلقاه المستهلكون.

مراقبة الجودة: ما هو "اختبار الإطلاق" الصيدلاني وما سبب أهميته؟
اليوم، تشرف إدارة الغذاء والدواء الأمريكية (FDA) على جودة ومحتوى $2.7 تريليون قيمة المنتج سنويا، ولكن يبدو أنه يقمع تقييمات ونتائج التحقق من المكونات الهامة. من المفترض أن تقوم إدارة الغذاء والدواء الأمريكية بحماية الأمريكيين من خلال إجراء شامل الاختبار التحليلي كمجموع اختباري لضمان دقة المكونات. ويجب أن تكون نتائج ذلك شفافة بالنسبة لدافعي الضرائب الذين يمولون هذا المشروع ادارة الاغذية والعقاقير 6.6 مليار دولار ميزانية. ويشار إلى هذا التحقق العلمي بأنه دوائي "اختبار الافراج". اختبار الإطلاق هو مصطلح تقني يشير إلى عملية تتضمن مجموعة متنوعة من التحليلات الآلية المستخدمة شامل منتجات اختبار للنقاء والتركيز والاتساق والهوية والشوائب من أي نوع.
وُلدت إدارة الغذاء والدواء بأكملها من ذلك الموظف "في قسم الكيمياء" منذ عام 1862 والحاجة إلى الشفافية والتحقق من المكونات. واليوم، انتشر هذا الموظف إلى قسم إدارة الغذاء والدواء بأكمله الذي يضم 1,300 عالم وموظف دعم من المفترض أنها مخصصة للتحقق من المكونات عبر اختبار الإطلاق الصيدلاني. ادارة الاغذية والعقاقير مكتب الجودة الصيدلانية (OPQ) من المفترض أن تتأكد من أن المستحضرات الصيدلانية تتطابق تمامًا مع محتويات المكونات المدرجة، دون تباين الجودة/الشوائب (نوعي) أو المحتوى (نوعي). القواعد التي تتطلب ذلك محددة للغاية ومفصلة 21 CFR § 201.10.
كيف تتحقق إدارة الغذاء والدواء من حقن mRNA لمراقبة الجودة:
كانت نتائج مراقبة الجودة من اختبارات حقن mRNA حاسمة بشكل خاص لأنها كبيرة ومعقدة وتم تصنيعها بسرعة. بينما يعتمد دافعو الضرائب على إدارة الغذاء والدواء للتحقق من جودة حقن mRNA ومشاركة النتائج، فإن إدارة الغذاء والدواء الأمريكية تعتمد على ذلك يبدو ملزمة بحماية مكونات الشركات المصنعة على حساب أبسط الشفافية فيما يتعلق بمنتجات mRNA Covid. وبينما يبدو أن إدارة الغذاء والدواء الأمريكية تقوم بجمع العينات، فإن منهجية "البريد" الخاصة بها معيبة بشكل أساسي. بالإضافة إلى ذلك، لا تشارك إدارة الغذاء والدواء الأمريكية نتائج تلك الاختبارات في أي مكان يمكنني تحديد موقعها فيه.
بمعنى آخر: أثناء الوباء عندما تم إطلاق طلقات الحمض النووي الريبوزي المرسال (mRNA) الجديدة والمنفذة على نطاق واسع على الأمريكيين "بسرعة هائلة" وعندما كانت أمريكا تعتمد على الجودة/الواجبات التنظيمية لإدارة الغذاء والدواء الأمريكية (FDA) أكثر من غيرها، كانت إدارة الغذاء والدواء الأمريكية (FDA) تقبل الرسائل "المرسلة بالبريد" ذاتيًا. في "اختبارات مراقبة الجودة و/أو النتائج. هل إدارة الغذاء والدواء الأمريكية لم تأخذ في الاعتبار ذلك؟ اعترف مصنعو mRNA بأنهم "يكافحون [د]" للاستجابة للتصنيع وكانوا "يسارعون" لمواكبة التصنيع مع عمليات التصنيع؟ وذكر مصنعو مكونات mRNA أيضًا أن الجهود المبذولة لتلبية الاحتياجات كانت "غير مسبوقة".
مثل هذه التصريحات لا تعطي ثقة المستهلك في الجودة، وتوضح الارتقاء الهائل بهذه المنتجات المعقدة التي ينبغي أن تضمن يقظة بشكل خاص والتدقيق الشخصي من قبل إدارة الأغذية والعقاقير (FDA) للمنشآت والمنتجات المصنعة، سواء كانت جائحة أم لا. على سبيل المثال، صرح أحد مصنعي مكونات mRNA أنهم قاموا فجأة بزيادة إنتاجهم بنسبة XNUMX٪ 50 أضعاف.
وفي خضم هذه التكنولوجيا الجديدة التي تم دفعها بسرعة "خاطفة"، لم يطالب أي من علماء OPQ البالغ عددهم 1,300 في إدارة الغذاء والدواء بإجراء عمليات تفتيش حية، أو على الأقل عرضوا القيام بأي شيء آخر غير طلب عينات "مرسلة بالبريد" قد تكون مشكوك فيها. للاختبار؟
السؤال الواضح هو: لماذا لم تجمع إدارة الغذاء والدواء العينات مباشرة؟؟ حتى مع انتشار الوباء، كان من الممكن أن تقوم إدارة الغذاء والدواء بتفتيش المنشآت مرتدية البدلات الخطرة أو - أو في جدا الأقل - اختيار جمع العينات من الصيدليات أو المستشفيات أو في مستودعات الموزعين.
المنهجية المخفية لاختبار مكونات حقن mRNA:
وبعيداً عن غياب نتائج الاختبارات ونتائج أخذ العينات "المرسلة بالبريد" المشكوك فيها، فإن إدارة الغذاء والدواء تفعل ذلك بالإضافة إلى ذلك إخفاء منهجيتهم التي تم التحقق منها ومنع الآخرين من إجراء تحليلاتهم المستقلة حول جودة/نقاوة حقن الرنا المرسال.
إن تحليل الأدوية بشكل مستقل من حيث النقاء والتلوث المحتمل مقارنة بقائمة المكونات هو شيء حاولت القيام به بنفسي عندما تصورت أول دواء في العالم. صيدلية تحليلية. ومع ذلك، نظرًا لأن لقطات mRNA هي تقنية جديدة تحتوي على قائمة مكونات أقل من الشفافية الكاملة، فإن منهجية الاختبار التي يحتاج المرء إلى استخدامها ليست واضحة كما هو الحال بالنسبة للأدوية الأخرى ذات الجزيئات الصغيرة. يتم حظر أي شخص يحاول البحث عن التخزين أو الاستقرار أو الخصوصية أو الكيمياء أو الحساسية أو حتى المنهجية الأساسية لاختبار التحقق من الصحة و/أو النتائج من خلال تقرير إدارة الغذاء والدواء الذي يحتوي على تنقيحات غازية بشكل مثير للسخرية، مما يجعل حتى الفهم العلمي الأساسي لكيفية التقييم المحتمل النتائج أو إجراء الاختبار مستحيل.
كمثال مرئي مؤثر، تعد صفحة واحدة منقحة في ملخص تنظيمي أطول لإدارة الغذاء والدواء (كما هو موضح أدناه) جزءًا من وثيقة 127 الصفحات (تمت مشاركة 63 صفحة فقط، ومن بين تلك الصفحات الـ 63، تم تنقيح حوالي 50٪ منها) حول كيفية تقييم النقاء والتركيز والمقاييس التحليلية الأخرى لحقن mRNA.
هؤلاء ادارة الاغذية والعقاقير (ب) (4) التنقيحات التنقيحات التفصيلية المحددة المستخدمة لـ "حماية الأسرار التجارية والمعلومات التجارية أو المالية السرية". ولكن هل من المناسب حقًا وصفه بأنه "تجاري" إذا تم تمويل البحث/التطوير/المنتج مئات الملايين من دولارات دافعي الضرائب?

بدون قائمة المكونات أو منهجية الاختبار، من المستحيل لأي شخص آخر خارج إدارة الغذاء والدواء الأمريكية أو الشركات المصنعة أن يعرف بدقة كيفية التحقق من المنتج. غش (المكونات المعدلة أو السامة) أو تسمية خاطئة (لأن القائمة الكاملة للمكونات (المكونات) بما في ذلك تسلسل النيوكليوتيدات و تكوينات الجسيمات الدهنية النانوية غامضة بشكل خاص على ملصق المنتج).
يعد الافتقار إلى المنهجية أمرًا مزعجًا بشكل خاص نظرًا لأن البيانات الأولية الجديدة التي تستخدم منهجية مستقلة أظهرت دليلاً على ذلك تلوث الحمض النووي في حقن mRNA Covid.
لذلك، إذا ادعى شخص خارجي أنه أجرى اختبارًا ووجد شوائب في لقطات mRNA وطلب من إدارة الغذاء والدواء أو الشركات المصنعة ردها، فسيتم مقابلته ببعض الردود التي تشير إلى شيء على غرار:
- لم تستخدم منهجية اختبار صحيحة/مناسبة للتوصل إلى استنتاجاتك، وبالتالي فإن تحليلاتك غير صالحة.
لذلك، سيحاول المختبر المستقل طلب منهجية الاختبار من الوثائق المعتمدة من إدارة الغذاء والدواء (أي الوثيقة الكاملة التي تحتوي على الشكل 5) بطرح السؤال التالي: “حسنًا، أرغب في اختباره باستخدام منهجيتك المعتمدة؛ هل ستخبرنا ما هذا؟"
- سترد إدارة الغذاء والدواء الأمريكية (FDA) أو الشركة المصنعة بشيء على غرار: "ما نحن على استعداد للكشف عنه حول المنهجية المستخدمة والتي ليست سرية يمكن العثور عليه عبر الإنترنت، أو من خلال طلب قانون حرية المعلومات التابع لإدارة الغذاء والدواء"... حيث سيتم مقابلتهم الوثيقة التالية المنقحة بشدة، حيث يتم تغطية أي شيء له معنى عن بعد بتنقيحات (ب)(4).
القراءة بين السطور: من الواضح أن الشركات المصنعة وإدارة الغذاء والدواء الأمريكية لا تريد أن يعرف أي شخص آخر المكونات الكاملة لحقن mRNA أو حتى اختبارها للتأكد من نقائها واتساقها.
وفقًا لمسؤولي إدارة الغذاء والدواء: تصنيع الأدوية هو جدا معرض للخطأ:
كثير من الممكن أن تسوء الأمور أثناء عملية تصنيع الأدوية. وبعيدًا عن التناقضات المحتملة مع حقن mRNA/LNP، فإن المشكلات النوعية والكمية تنطوي على ذلك. كل منتج صيدلاني خاضع لرقابة إدارة الغذاء والدواء. وحتى مجلسا النواب والشيوخ اعترفا رسميا بالتقارير التي تتحدث عن فشل إدارة الغذاء والدواء في تأمين سلسلة توريد الأدوية الأمريكية. الأغلبية الصيدلانية الامريكية منتج المستهلك والمستخدم النهائييتم إنتاجها في الخارج في دول مثل الهند والصينوغيرها من البلدان ذات تكلفة العمالة المنخفضة ليس يحظى بتقدير جيد لمستويات عالية من مراقبة الجودة. السجل الفيدرالي مليء بالتقارير الانتهاكات في المصانع الهندية والصينية.
هل تقوم إدارة الغذاء والدواء أيضًا بالتصديق على هذه النباتات - بما في ذلك تلك التي لها تاريخ طويل من الانتهاكات - عبر نظام "البريد" إلى إدارة الغذاء والدواء؟ ومن المثير للغضب أن الإجابة على هذا السؤال هي أمر من شأنه أن يجعل أي شخص مهتم بالجودة الصيدلانية غير مرتاح للغاية.
في حين أن ستة سيغما لقد كان مستوى الدقة منذ فترة طويلة هدفًا للجودة والسلامة في السيارات والكمبيوتر والهواتف المحمولة وغيرها من الصناعات ذات التقنية العالية، ويبدو أنه تم تجاهله في الغالب عندما يتعلق الأمر بتصنيع الأدوية.
نشر مسؤولو إدارة الأغذية والعقاقير (FDA) بيانات تقدر عدم الدقة بـ 2-3σ (سيجما) في تصنيع الأدوية. جودة 2σ تقابل 308,537 عيبًا لكل 1,000,000 فرصة. (من المحتمل أن يكون هناك أكثر من مليون فرصة للخطأ عندما يتعلق الأمر بتصنيع الأدوية). وتدرك إدارة الغذاء والدواء الأمريكية هذا الأمر على أعلى مستويات القيادة؛ في الواقع، الحالي رئيس مكتب الجودة الدوائية في إدارة الغذاء والدواء، مايكل كوبشا حتى أنه كتب ونشر حساب ستة سيجما أعلاه، معربًا عن أسفه للطبيعة غير الدقيقة لتصنيع الأدوية ظهر في 2017.
يمكن أن يكون خط عرض الخطأ لمنتجات mRNA و/أو LNPs الخاصة بها متساويًا أقل دقيقة من 2-3σ، (كلما كانت σ أقل، كان المنتج أكثر خطأً) نظرًا لأنها تحتوي على مادة نيوكليوتيدات وLNPs جديدة، مما يجعلها أكثر تعقيدًا إلى حد كبير من المستحضرات الصيدلانية ذات الجزيئات الصغيرة - على الرغم من تطويرها وتصنيعها وإطلاقها في " سرعة الاعوجاج."
حتى مع اعتراف إدارة الغذاء والدواء ومسؤوليها بوجود عدم دقة متأصلة في التصنيع، لماذا في عالم الرياضة الواسع فهل لا تفي إدارة الغذاء والدواء بمهمتها المتعلقة بالسلامة من خلال مشاركة اختبارات إطلاق تكنولوجيا mRNA علنًا مع الجمهور الأمريكي الذي يمولها؟
ما قبل 1862 مرة أخرى؟ هل لقطات mRNA هي الأدوية الوحيدة التي لا يملكها الأمريكيون؟ كامل معلومات المكونات؟
إن عدم الوضوح بشأن عدد تسلسلات لقطات mRNA وغيرها من المعلومات المهمة يتناقض بشكل مباشر مع دواء آخر يعتمد على الحمض النووي الريبي (RNA) معتمد من إدارة الغذاء والدواء الأمريكية - باتيسيران (Onpattro®). توفر Onpattro بشفافية التسلسل والوزن الجزيئي وقوة الملليجرام لمنتجاتها ضمن إدارة الغذاء والدواء الرسمية وضع العلامات على الحزمة كما هو موضح في المقتطف أدناه:


عدم وجود خصوصية جرعة Covid mRNA: 0.3 مل (أو 0.5 مل) ماذا?
حتى الآن، ما زلنا لا نملك معلومات أساسية عن المكونات المتعلقة بأي حقن لفيروس Covid mRNA. الصيادلة يعرفون فقط إعطاء محددة حجم من السوائل، ويبدو أنه فعل ذلك دون سؤال. عادةً، يجب أن توضح الملصقات الرسمية على عبوات إدارة الغذاء والدواء تفاصيل المكونات الفعلية في هذا الحجم، ولكن ليس بالنسبة لملصقات Covid mRNA: فهي تشير ببساطة إلى 0.3 مل (أو 0.5 مل) باسم "شكل الجرعة والقوة".
بالإضافة إلى ذلك، كما يمكن لأي طالب في المدرسة الثانوية أن يخبرك، فإن 0.3/0.5 مل هو XNUMX/XNUMX مل حجمليس قوة. لا نعرف أي تفاصيل كمية لما هو موجود في 0.3/0.5 مل مثل: كم عدد جزيئات LNP؟ ما حجم/مورفولوجيات تلك LNPs؟ كم عدد تسلسلات mRNA في هذا المجلد؟




هل هذا ما يعتبر شفافًا بدرجة كافية أو "تصنيفًا صادقًا" من قبل إدارة الغذاء والدواء؟
إن مقتطف القص واللصق أعلاه من ملحق العبوة هو جميع المعلومات التي تشاركها الشركات المصنعة مع المستهلكين فيما يتعلق بالجرعة - وهي غير كافية على الإطلاق مقارنة بجميع ملصقات إدارة الغذاء والدواء الأخرى - أو أي شخص لديه فضول لمعرفة أي شيء يتجاوز مقدار السوائل للحقن وتركيز 30 أو 100 ميكروغرام من تسلسل mRNA غير محدد.
يبدو أن عدم الدقة الملحوظة في هذا التصنيف الذي سمحت به إدارة الغذاء والدواء يتعارض مع التصنيف الذي يبلغ عمره 120 عامًا تقريبًا على وجه التحديد: "اشتراط أن تحمل الأغذية والأدوية بيانات وصفية صادقة وأن تستوفي معايير معينة للنقاء والقوة".
هل هذه هي القائمة "الصادقة" للمكونات التي وضعتها إدارة الغذاء والدواء؟ (يرى 21CFR §352و 21 CFR §201.10 فيما يتعلق بـ "بيان المكونات" و"الأدوية والأجهزة ذات العلامات التجارية الخاطئة.")
والسؤال هو: هل يتم إدراج مكونات غير معروفة أو غير محددة لا يمكن لأي شخص باستثناء الشركة المصنعة فك شفرتها؟ في الحقيقة تلبية الروح أو المتطلبات القانونية لـ "وضع العلامات؟" فهل هذه التسمية هي التي تعتبرها إدارة الغذاء والدواء الأمريكية "صادقة"؟ على أي حال تقف إدارة الغذاء والدواء على أي حال؛ المصنعين أو المستهلكين؟
بالإضافة إلى أنه لم يتم تحديده بشكل مباشر، لا يمكن حتى استقراء العدد الدقيق لشرائط LNP أو mRNA في حقنة 30 أو 100 ميكروجرام بشكل متكافئ أو على أساس رقم أفوجادرو، لأن تسلسل mRNA، والوزن الجزيئي، و/أو مكون/تكوينات LNP غير متوفرة في أي مكان ضمن التصنيف الرسمي لإدارة الغذاء والدواء.
كيف يمكن لأي شخص معرفة ما إذا كان عدد خيوط mRNA لتشفير البروتين الشوكي لكوفيد يتناسب مع حمل لقاح كوفيد الذي يمكن أن يتلقاه الشخص من عدوى مكتسبة من المجتمع؟ إجابة: لا يستطيعون.
هل حقن Covid mRNA تم تصنيفها بشكل مناسب/تسميتها بشكل خاطئ?
21 211.125 CFR يحدد "يجب ممارسة رقابة صارمة على الملصقات الصادرة للاستخدام في عمليات وضع العلامات على المنتجات الدوائية،"ولكن يبدو أن إدارة الغذاء والدواء كانت متساهلة للغاية فيما يتعلق بوضع العلامات المعتمدة على حقن Covid mRNA على الرغم من ذلك وكل دواء آخر - بما في ذلك دواء Onpattro القائم على mRNA - يحدد هذه المعلومات. تاريخيًا، كانت القرارات التنظيمية لإدارة الغذاء والدواء (مثل المعلومات التي يجب تضمينها في ملصقات المنتجات) تعتمد على الأسبقية، وكانت لقطات Covid mRNA انحرافًا واضحًا عن الأسبقية التاريخية والقانونية لإدارة الغذاء والدواء. يعود هذا الغياب الملحوظ للبيانات والافتقار إلى الوضوح إلى أيامنا هذه مورلي الكبد والكلى ودية في أواخر 1800s. والفرق هو: في ذلك الوقت، لم تكن إدارة الغذاء والدواء موجودة، ولكن اليوم هناك إدارة الغذاء والدواء تضم ما يقرب من 20,000 ألف موظف، على الأقل بعضهم يعتقد ظاهريًا أن هذه التسمية شفافة و"صادقة".
إن ذكر مكون غير معروف / غير قابل للفك / غامض ولا يمكن لأحد أن يحدده بدقة على الأرجح ليس هو ما قصده المشرعون في قانون الغذاء والدواء النقي لعام 1906 عندما حددوا قواعد إدارة الغذاء والدواء بشأن "التوسيم الصادق". ويفصل عن ذلك: حقيقة أن الجرعات مضاعفة لكل حجم من الشركات المصنعة المختلفة (30 ميكروجرام/0.3 مل vs 100 ميكروجرام/0.5 مل) يعني أن تسلسلات mRNA هذه تبدو مختلفة إلى حد كبير في طول النوكليوتيدات، وهذا بدوره سيكون مختلفًا المزيد ومختلف LNPs بالإضافة إلى المرفقات. هل هذا يعني أن تسلسلات mRNA المستخدمة في نسخ بروتين السنبلة يبلغ حجمها ضعف الحجم (10 ميكروجرام/0.1 مل مقابل 20 ميكروجرام/0.1 مل) مقارنة بالمصنعين المختلفين، أم أن هناك شيئًا آخر يساهم في اختلاف طول النوكليوتيدات؟
بالنسبة للشخص العادي الذي لا يزال يقرأ حتى هذه النقطة (مجد، بالمناسبة): يمكن أن يكون الافتقار إلى معلومات مفصلة عن العلامات مثل الإعلان على نطاق واسع عن منزل للبيع، موضحًا أنه مصنوع من الخشب والطوب، على لوح أسمنتي - ولكن لا يظهر أي صور للمنزل (مثل التسلسل) وعدم مشاركة لقطاته المربعة (مثل الوزن الجزيئي). وعلى أية حال، فإن نقص المعلومات غير كاف وانحراف عن المعايير التقليدية.
يحتوي كل دواء آخر معتمد من إدارة الغذاء والدواء - بما في ذلك أدوية mRNA الأخرى - على إفصاحات كاملة عن المكونات في منتجاتها، بما في ذلك التمثيل الهيكلي والوزن الجزيئي لمنتجاتهم حتى يعرف الناس بالضبط ما سيحصلون عليه.
هذا صحيح: ابحث عن أي دواء يمكن أن يخطر ببالك في قاعدة بيانات Drugs.com ولاحظ كيف توفر جميع الملصقات البنية و/أو الوزن الجزيئي. دليل على أن لقطات Covid mRNA هي واضح استثناء لممارسة موافقة إدارة الغذاء والدواء التاريخية وقاعدة "العلامة الصادقة".
دراسة دنماركية لعام 2023 توضح تفاصيل التباين السريري الكبير بين دفعات حقن mRNA Covid-19 mRNA:
يبدو أن عدم وجود أي شفافية بشأن التحقق من صحة الاختبار "المرسل بالبريد" الذي يحتمل أن يكون غير صالح قد منح الشركات المصنعة تصريحًا لجزء آخر مهم للغاية مما تشرف عليه إدارة الغذاء والدواء: المظاهر السريرية المحتملة على اختلافات الدفعة/الدفعة من لقطات mRNA. بأثر رجعي دراسة السلامة الدنماركية تم نشره في وقت سابق من عام 2023 بالتفصيل نمطًا منحرفًا للغاية لتقارير الأحداث الضارة من حقن Pfizer-BioNTech BNT162b2 mRNA كما يرتبط بنظام الإبلاغ عن الأحداث الضارة الدنماركي DKMA.
في الرسم البياني الخطي التالي، تمثل النقاط الملونة المختلفة دفعات مختلفة من حقن mRNA الخاصة بشركة Pfizer-BioNTech. قامت بفصل الدفعات إلى ثلاث فئات مختلفة؛ عدد مرتفع - منخفض - إلى (تقريبًا) غياب لمجموعات الأحداث الضارة المُبلغ عنها (المؤامرات الزرقاء والخضراء والصفراء على التوالي).
بعبارات أخرى: يبدو أن المنتجات "المكافئة" المفترضة من نفس الشركة المصنعة لها حالات مختلفة تمامًا من الأحداث الضارة، حسب الدفعة، حيث تمثل كل دفعة من هذه الدفعات مئات الآلاف من حقن mRNA.
عند إضافة خطوط الانحدار الخطي المقابلة، ظهر نمط معين:
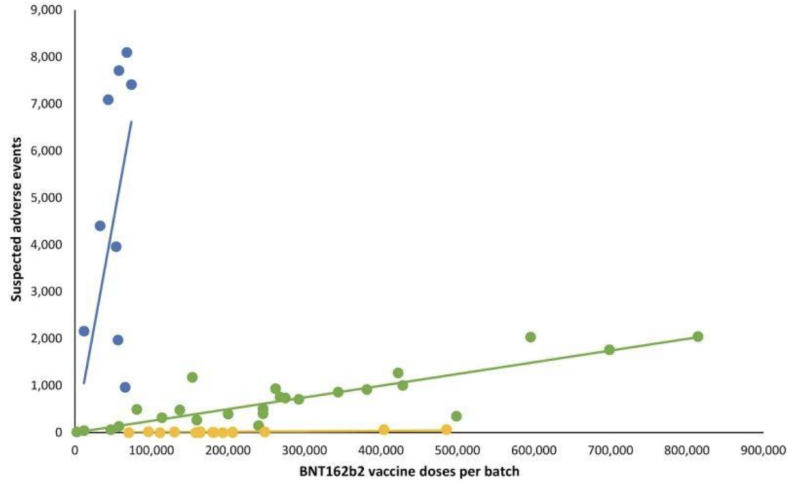
تتضمن الأسئلة المهمة حول تباين الأحداث السلبية الجديرة بالملاحظة بين دفعات Covid-19 mRNA ما يلي:
- هل يمكن أن تكون تباينات الأحداث الضارة ناتجة عن تباينات نوعية أو كمية في تسلسلات الرنا المرسال أو عدد خيوط الرنا المرسال بين الدُفعات؟
- هل يمكن أن تكون فروق الأحداث الضارة بسبب الفروق النوعية أو الكمية في الحجم/التشكل أو كمية LNPs بين الدُفعات؟ ما هي الاختبارات التي تم إجراؤها ل ضمان سلامة LNPs المختلفة المستخدمة في حقن mRNA؟
- هل كانت تلك الدفعات التي تتوافق مع نقاط البيانات الصفراء مقابل الخضراء مقابل الزرقاء مختلفة نوعًا ما أو كميًا؟
- هل تم اختراق التخزين/المناولة بعد التصنيع في المنشأة الإدارية (أو في مكان آخر على طول سلسلة التوريد) مما أدى إلى تقلب المنتج؟
- ما هو معدل سيجما/الخطأ لهذا المنتج وغيره من المنتجات التي تنشأ من منشأة التصنيع المعينة/رئيس المناوبة المسؤول عن التصنيع؟
- هل تم الحصول على مكونات منتجات Covid mRNA من الهند أو الصين مقابل أي مكان آخر، اعتمادًا على الدفعة؟
- ما هي النسب المئوية لدفعات منتجات Covid mRNA التي تم اختبارها من خلال التجميع الشخصي بواسطة مفتش إدارة الغذاء والدواء مقابل "إرسالها بالبريد" منذ البداية حتى الآن؟ هل تم اختبار كل دفعة باستخدام إحدى طريقتي التجميع هاتين فقط؟
- هل قامت إدارة الغذاء والدواء الأمريكية (FDA) بإجراء التحقق من اختبار الإصدار على مجموعات نظام الإبلاغ عن الأحداث الضارة في DKMA الدنماركية؟ إذا كانت الإجابة بنعم، فلماذا لا تنشر إدارة الغذاء والدواء نتائج الاختبارات المحددة هذه؟ إذا لم يكن الأمر كذلك، لماذا لم يتم إجراء الاختبار؟
- هل هناك مشكلة أساسية في إنتاج LNPs و/أو تسلسلات mRNA باستمرار بشكل موثوق ودون تلوث؟
يمكن البدء في معالجة نتائج الدراسة الدنماركية والأسئلة المذكورة أعلاه حول الأحداث السلبية، ولكن ليس بدون مشاركة إدارة الغذاء والدواء الأمريكية بشكل مستقل لنتائج اختبار الإطلاق. في الوقت الحالي، بسبب تنقيحات إدارة الغذاء والدواء (ب) (4) المنتشرة في كل مكان، لا أحد يعرف المنهجية المعتمدة لاختبار لقاحات Covid mRNA or بالضبط ما هي القطع في الدراسة الدنماركية التي تم اختبارها أو لم يتم اختبارها or نتائج تلك الاختبارات الدفعية.
… ثم مرة أخرى، حتى لو اختارت إدارة الغذاء والدواء الأمريكية إصدار نتائج اختبار الدفعات هذه، فكيف يمكن للمستهلكين معرفة ما إذا كانت هذه النتائج تمثل دفعات محددة، نظرًا لأن الشركات المصنعة تختار بنفسها العينات التي سيتم إرسالها بالبريد؟
يعد عدم توفير شفافية المكونات وضمان الجودة من خلال منهجية أخذ العينات المناسبة مطلبًا أساسيًا وأساسيًا لإدارة الغذاء والدواء. وفي الحقيقة كان السبب الرئيسي في إنشاء هيئة الغذاء والدواء! ألا يستحق الأمريكيون قوانين أفضل للشفافية والرقابة و"التوسيم الصادق" عندما يتعلق الأمر بمستحضراتنا الصيدلانية - خاصة وأن هذه القوانين صدرت قبل أكثر من 100 عام؟
نشرت تحت أ ترخيص Creative Commons Attribution 4.0
لإعادة الطباعة ، يرجى إعادة تعيين الرابط الأساسي إلى الأصل معهد براونستون المقال والمؤلف.









